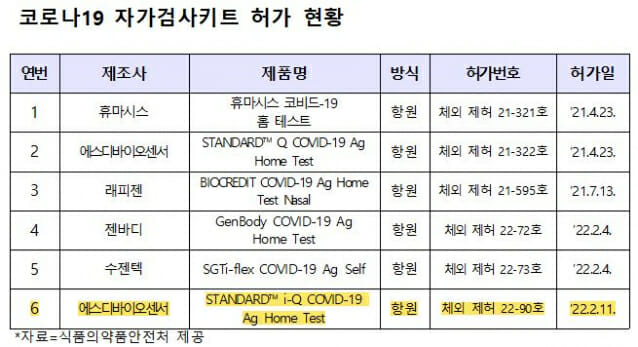
식품의약품안전처는 개인이 직접 코안(비강)에서 검체를 채취해 바이러스 감염 여부를 확인하는 항원검사 방식의 코로나19 자가검사키트 1개 제품을 2월11일 추가로 허가했다.
이번에 허가한 자가검사키트는 에스디바이오센서㈜가 두 번째로 허가받은 ‘STANDARD i-Q COVID-19 Ag Home Test’ 제품이며, 자가검사키트 허가기준인 민감도(질병이 있는 환자 중 검사결과가 양성으로 나타날 확률) 90% 이상과 특이도(질병이 없는 환자 중 검사결과가 음성으로 나타날 확률) 99% 이상을 충족한 것으로 나타났다.
자가검사키트는 전문가가 아닌 개인이 직접 코로나19 검사를 할 수 있는 진단시약으로, 결과가 양성일 경우 선별진료소 등에 방문해 유전자 검사(PCR)를 받아야 한다. 또 사용한 검사키트(양성)는 제품에 동봉된 봉투에 밀봉해 선별진료소 등에 가져가서 처리해야한다.
식약처는 자가검사키트 생산업체와 긴밀하게 협의해 충분한 물량이 국내에 공급될 수 있도록 관리하고 있으며, 앞으로도 지속적으로 자가검사키트 공급 물량을 충분히 확보해 공급할 예정이므로 개인이 미리 과다하게 구매하실 필요가 없다고 설명했다.
관련기사
- 홈앤쇼핑, 코로나19 자가검사키트 판매 방송 진행2022.02.11
- 씨젠, 브라질에 400만명 검사 분량 진단시약 수출2022.02.10
- 식약처, 코로나19 자가검사키트 2개 품목 허가2022.02.04
- PCR검사, 고위험군 등 우선…자가검사키트 수급 문제 없어2022.02.03












