암의 전이가 조절되는 유전자 경로가 밝혀져 이를 막는 새로운 치료기술 개발이 가능해질 전망이다.
미래창조과학부는 한국원자력의학원 엄홍덕 박사팀이 암세포에서 변이가 자주 관찰되는 complex I 효소와 p21 단백질을 통해 암 전이가 조절되는 경로를 밝혀, 암세포 전이를 막는 새로운 치료기술 개발의 가능성이 열렸다고 2일 밝혔다.
암 전이는 암세포가 원래 발생한 조직이나 장기로부터 다른 조직이나 장기로 이동하는 것을 말한다. 특히 ‘두 번째 암’으로 불리는 전이암은 치료 방법이 제한적이거나 치료효과가 낮은 경우가 많고, 암 전이가 일어나는 원리에 대해 밝혀진 바가 거의 없어 극복에 어려움이 있었다.
지난 1997년부터 2011년까지 국가암등록통계에 따르면, 암 환자 생존율이 66.3%인데 반해, 전이암 생존율은 18.7%에 불과할 정도다.
엄홍덕 박사팀은 폐암 세포와 쥐를 이용한 동물실험을 통해 complex I 효소가 암 전이를 촉진하는 핵심 인자임을 처음으로 밝히고 이 효소의 조절 경로를 확인했다.
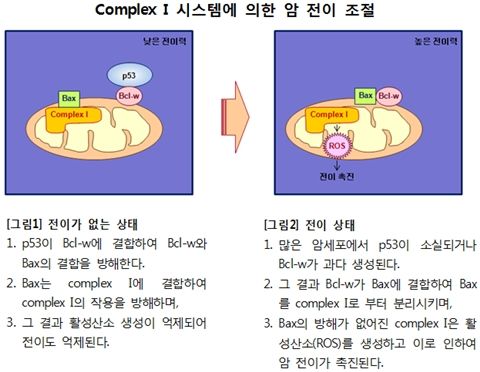
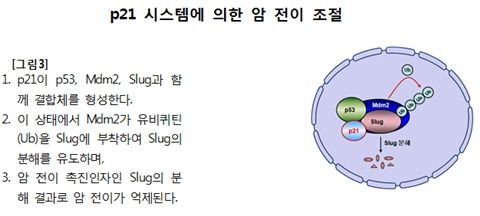
complex I 효소는 활성산소 생성을 통해 암 전이를 촉진하는데, 이러한 전이 과정은 세포 사멸 단백질로 알려진 ‘Bax 단백질’을 통해 제어되며, Bax 단백질은 다시 다른 단백질들과 결합을 통해 암의 전이를 조절 경로를 규명함으로써 암 전이 제어기술의 개발이 가능해 졌다.연구팀은 또한 세포 성장을 조절하는 것으로 알려진 p21 단백질이 암 전이를 촉진하는 물질(slug)을 분해함으로써 암 전이를 억제하는 것과 이 과정에 관여하는 여러 단백질들의 분자적 결합과정도 처음으로 규명했다.
p21 단백질은 암 억제 인자로 유명한 p53을 비롯한 다른 단백질들과 거대 결합체를 형성해 slug를 분해하는 것으로 나타났으며, 특히 이 과정에서 p21과 p53의 협력성은 학계의 비상한 관심을 받고 있다.
이번 연구를 통해 암 전이를 촉진하는 작용은 억제하고, 암 전이를 억제하는 작용은 상승시키는 다양한 치료법의 실용화 가능성이 열렸으며, 향후 환자의 유전적 특성에 따른 암 전이 예방을 기대할 수 있게 됐다.
Complex I 시스템에 변이가 일어난 환자와 p21 시스템에 변이가 생긴 환자를 구분해 각각에 적합한 암 전이 억제 치료법 및 치료기술의 개발이 가능해 진 것이다.
미래창조과학부에서 지원하는 방사선기술개발사업의 일환으로 수행된 이번 연구 결과는 이달 세계적 권위의 분자생물학과 암 생물학 학술지인 ‘EMBO Reports’와 ‘Oncotarget’에 두 편의 논문으로 게재됐다.
이번 연구는 암의 전이가 일어나는 새로운 핵심 경로를 밝혀 암 극복을 위한 새로운 기술 개발의 가능성을 열었다는 관점에서 그 의미가 크다.
엄홍덕 박사는 “그간 암 환자에서 complex I과 p21의 변이가 많이 관찰됐으나 그 의미를 정확히 알기는 어려웠다”며 “이번에 규명된 전이 경로를 바탕으로 암 전이 억제를 극대화하는 물질이나 기술을 개발하면 암 전이를 사전에 차단해 암환자 생존율 향상에 크게 기여할 것”이라고 내다봤다.
[주요 용어]
complex I - 세포 속의 미토콘드리아에 위치하는 거대 효소로서 세포의 에너지 대사에 관여함
p21 - 세포 성장을 조절하는 단백질
Bax 단백질 - 결함이 있거나 체내에서 필요가 없어진 세포를 죽이는 단백질
p53 : 가장 대표적인 암 억제 단백질
Slug : 암 전이 촉진 단백질
Bcl-w : 세포사멸 억제 단백질
관련기사
- 국립암센터, 시스코UCS-VM웨어 기반 VDI 구축2014.09.02
- 국내서 세계 최초 암치료 나노로봇 개발2014.09.02
- 암세포 공격 ‘자연살해세포’ 감소원리 규명2014.09.02
- 암 증식 전이 억제약물 분자표적 규명2014.09.02
Mdm2 : 단백질 분해 유도 효소
활성산소 : 강력한 산화력을 보유한 산소의 불완전한 환원체. 세포내에서 아주 다양한 경로를 통해 생성될 수 있지만 에너지를 생성하는 미토콘드리아 호흡의 부산물로 주로 생성되는 것이 가장 대표적임. 생성된 활성산소는 그 양과 생성 기간에 따라 세포 사멸, 노화 등을 유도할 수 있다고 알려져 있음.