정상 세포는 건드리지 않고 질병 세포만 찾아 교정하는 유전자 가위 시스템이 개발됐다. 표적 유전자가 아닌 다른 유전자를 편집할 위험이 있다는 유전자 가위의 문제를 해결할 수 있으리란 기대다.
KAIST(총장 이광형)는 의과학대학원 이지민 교수 연구팀이 한국과학기술연구원(KIST) 오승자 선임연구원, 강원대학교 이주용 교수와 공동 연구를 통해 질병 세포에서만 핵 내 유전자 교정을 수행하는 유전자 가위 시스템(CRISPR/Cas9)을 개발했다고 14일 밝혔다.
질병 세포에서는 마이크로RNA가 과다 발현된다는 점에 착안, 유전자 가위 시스템에 마이크로RNA에 의해서만 절단되는 링커를 연결했다. 이렇게 설계된 시스템은 마이크로RNA가 적은 정상 세포에서는 세포질에 머물며 유전자 교정을 수행하지 않지만, 질병 세포에서는 링커가 절단되면서 풀려난 유전자 가위가 세포핵 안으로 들어가 유전자 교정을 수행한다.
유전자 가위를 질병 세포에서만 기능할 수 있게 해 정상 세포와 질병 세포가 혼합돼 있는 실제 환자에게 효과적으로 유전자 교정 치료를 할 수 있다.
마이크로RNA는 유전자 전사 후 조절하는 역할을 한다. DNA로부터 전사된 메신저 RNA에 아르고너트(Ago) 단백질을 통해 결합하며, 결합한 메신저 RNA를 절단한다. 여러가지 질병이 마이크로RNA의 비정상적인 발현과 연관된 것으로 알려져 있어, 질병 치료를 위한 표적 바이오마커로 많이 연구되고 있다.
연구진은 마이크로RNA가 메신저 RNA 표적 서열을 절단하는 특성을 활용, 핵 위치 신호(NLS)가 부착된 기존 유전자 가위(Cas9)에 핵 외 수송신호(NES)가 연결된 메신저 RNA 표적 서열을 결합했다. 이렇게 만든 유전자 가위에 '셀프 체크인'이라는 이름을 붙였다.
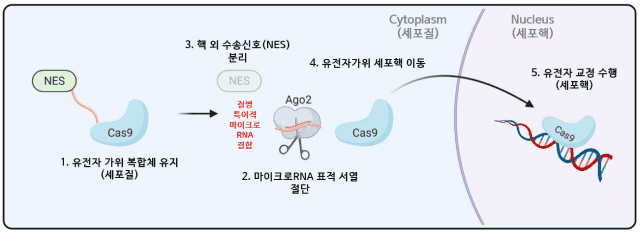
이 유전자 가위의 마이크로RNA 표적 서열은 마이크로RNA에 의해 잘라진 후 핵까지 전달되어 유전자 가위 기능을 수행했다.
폐암 세포에서 과발현되는 마이크로RNA-21과 그 표적 서열로 만든 유전자 가위로 실험한 결과, 폐암 세포에 있는 발암 유전자 Ezh2를 교정할 수 있음을 확인했다.
관련기사
- 유전자 가위, AIDS 치료제 개발 문 열다2022.03.14
- 유전자 가위로 부작용 없는 암 치료법 개발2022.02.23
- 정밀 방사선 치료, 전이암 치료율 높여2022.04.21
- 나프타 쇼크에 포장재 비상…파우치 배터리는 괜찮나2026.03.28
이 유전자 가위는 마이크로RNA에 의한 표적 서열 절단이라는 세포 내 시스템을 활용한다는 점에서 안정성이 높고, 세포 독성도 줄일 수 있을 것으로 연구진은 내다봤다.
이 연구는 학술지 '뉴클레익 에시드 리서치(Nucleic Acids Research)' 온라인판에 최근 실렸다.