KAIST(총장 이광형)는 박현규 생명화학공학과 교수 연구팀이 유전자 가위의 일종인 크리스퍼-카스12a(CRISPR-Cas12a) 시스템의 부수적 절단 활성을 활용해 RNA 분해효소를 민감하게 검출하는 신기술을 개발했다고 14일 밝혔다.
Cas12a 단백질은 표적 DNA 서열을 인식해 이를 절단하며, 이에 더해 주변의 비표적 단일 가닥 DNA를 무작위로 절단하는 부수적 절단 활성을 갖는다. 이러한 성질은 분자진단 분야에서 활발하게 쓰이고 있다.
연구진은 RNA 분해효소의 일종인 리보핵산가수분해효소 H를 현재 보고된 기술 중 가장 높은 민감도로 1시간 안에 검출하는 방법을 찾았다.

리보핵산가수분해효소 H는 후천성면역결핍증(AIDS)을 일으키는 인간 면역결핍 바이러스(HIV-1)나 B형 간염 바이러스 등 역전사 바이러스의 역전사효소에서 필수적인 영역으로, 역전사 바이러스의 증식에 관여한다. 따라서 리보핵산가수분해효소 H는 항바이러스제 개발의 중요한 표적으로 알려져 있다.
통상 리보핵산가수분해효소 H의 활성을 검출하기 위해서는 전기영동 또는 고성능 액체크로마토그래피 등의 방식을 사용한다. 하지만 이런 방법은 특이도와 민감도가 낮고, 검출 과정이 복잡하고 오래 걸린다는 단점이 있다.
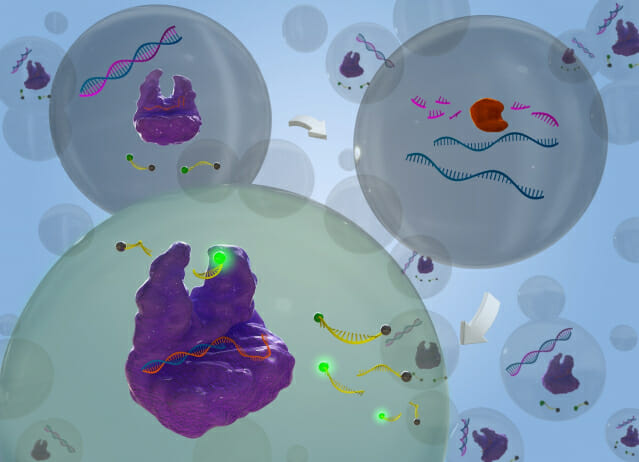
연구팀은 리보핵산가수분해효소 H의 기질로 짧은 DNA/RNA 키메라 복합체를 활용, 리보핵산가수분해효소 H의 활성 하에 활성제 DNA(Activator DNA, AD)가 방출되도록 설계했다. 유전자 가위의 Cas12a/crRNA 복합체가 방출된 활성제 DNA를 인식하면 Cas12a의 부수적 절단 활성을 가동해 주변의 리포터 DNA를 절단해 형광 신호가 발생하도록 설계했다. 이를 통해 표적 유전자 돌연변이를 고감도로 정확하게 검출할 수 있었다.
연구팀은 이 기술로 암세포의 리보핵산가수분해효소 H 활성도 성공적으로 검출할 수 있었다.
리보핵산가수분해효소 H가 인간 면역결핍 바이러스 증식에 관여한다는 점을 고려할 때, 이번 연구 성과는 에이즈 치료제 개발에 기여할 것으로도 기대된다.
관련기사
- 걱정되는 유전자 편집 부작용, 확 줄일 방법 찾았다2022.03.03
- 유전자 가위로 부작용 없는 암 치료법 개발2022.02.23
- 국내 PCR 검사로 ‘오미크론’ 잡아낸다2021.11.29
- 월드 랠리서 만난 현대차 vs 토요타…"여기선 빠른 제조사가 1위"2024.11.22
박현규 교수는 "이번 기술은 CRISPR-Cas12a 시스템의 부수적 절단 활성을 활용해 리보핵산가수분해효소 H를 고도로 민감하게 검출, 항바이러스제의 표적 발굴에 활용될 수 있다"라고 설명했다.
이번 연구는 경찰청의 치안과학기술연구개발사업 및 한국연구재단의 중견연구자지원사업과 바이오·의료기술개발사업의 일환으로 수행됐다. KAIST 생명화학공학과 김한솔 박사가 제1 저자로 참여한 이번 연구는 학술지 '케미컬 커뮤니케이션스(Chemical Communications)' 2022년 16호 표지 논문으로 최근 선정됐다.









