건국대학교는 의학전문대학원 유정수 교수 연구팀이 종양 억제 유전자로 알려진 ‘SMARCB1’이 간암에서는 종양을 유발할 수 있다는 사실을 최초로 규명했다고 22일 밝혔다. 연구팀은 이같은 분자생물학적 기전과 이를 억제할 수 있는 치료전략도 함께 제시했다.

한국연구재단 기초연구사업 신진연구자지원사업 지원으로 진행한 이번 연구 성과는 미국 암학회(American Association for Cancer Research)에서 편찬하는 종양학 분야 상위 7.58% 학술지인 ‘Cancer Research(IF 9.727)’에 지난 17일 온라인으로 게재됐다.
간암은 주요 원인인 B형 간염 백신과 항바이러스제가 개발되면서 감소할 것으로 예상했으나, 여전히 높은 사망률을 기록하고 있다. 특히 40~50대 중년 연령대에서는 전체 암 사망률 1위를 차지한다.
연구팀에 따르면 최근 차세대염기서열분석(NGS) 등 기술 발달과 세계 유전체 컨소시엄의 활발한 활동으로 크로마틴 리모델러(ATP를 사용해 염색질인 크로마틴 구조를 변화시키는 단백질 복합체)들의 많은 유전학적 변이와 비정상적인 발현이 많은 암에서 보고되고 있지만, 그 역할과 근본적인 작용 메커니즘은 아직 잘 이해되지 않고 있다.
유 교수팀은 크로마틴 리모델러의 서브유닛이며, 기존에 종양억제유전자로 알려진 SMARCB1이 간암에서 어떤 역할을 하는지 조사한 결과 SMARCB1이 간암 환자에서 고도로 상향 조절되며 불량한 예후와 관련이 있음을 확인했다.
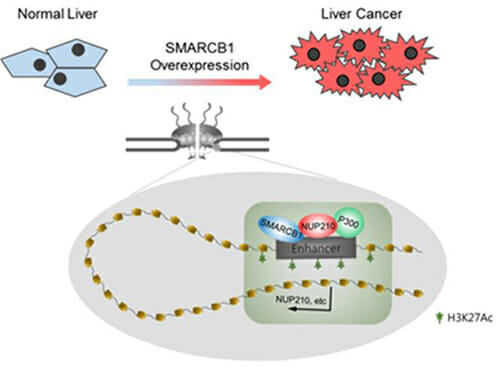
연구팀은 SMARCB1 손실에 따른 유전자 발현과 크로마틴 결합을 기반으로 한 SMARCB1와 H3K27Ac의 포괄적인 분석 결과, 핵막 단백질 NUP210이 간암에서 SMARCB1의 주요 표적임을 밝혔다. SMARCB1이 핵막단백질 NUP210 인핸서(Enhancer, 유전자 발현 DNA 조절 부위)에 결합하면 H3K27Ac의 농축 및 유전자를 발현해 콜레스테롤 항상성과 이종생물대사의 변화를 조절하고 NUP210은 간암에서 새로운 종양 지지체가 될 수 있음을 밝혀냈다.
관련기사
- 건국대 무역전문가과정 학생, 상금 등 모아 1천만원 기부2021.01.11
- 건국대 김성영 교수팀, AI 기반 혈관 노화 유전체 지도 구축2020.12.21
- 건국대 연구팀, 장애물 충돌해도 추락 않는 비행로봇 개발2020.12.09
- 건국대 2021 정시 평균 경쟁률 5.64 대 12021.01.11
SMARCB1의 과발현은 NUP210 인핸서에 크로마틴 구조 변화를 야기하고 이는 비정상적인 유전자 발현을 유도해 간암 발생 및 유지에 기여하게 된다.
유정수 교수는 “종양을 억제하는 유전자로 알려진 SMARCB1이 간암에서는 크로마틴 구조 변화를 일으켜 간암 발생과 유지하는데 기여하는 기전을 규명했다”며 “크로마틴 리모델러 유전적 변이나 비정상적 발현을 가지는 여러 암 치료제 개발에도 활용할 수 있을 것”이라고 말했다.












