국내에서 개발한 키메라 항원 수용체(CAR) T 치료제가 허가됐다.
식품의약품안전처는 큐로셀이 개발한 ‘림카토주’(안발캅타젠오토류셀)를 허가했다고 밝혔다.
키메라 항원 수용체(CAR, Chimeric Antigen Receptor) T 치료제는 환자의 면역세포를 유전적으로 조작해 암세포를 정확히 찾아 공격하도록 만든 개인 맞춤형 유전자치료제이다.
림카토주는 두가지 이상의 전신 치료 후 재발하거나 반응이 없는(불응성) 미만성 거대 B세포 림프종 및 원발성 종격동 B세포 림프종 성인 환자를 치료하는 희귀의약품이다. 환자의 면역세포(T세포)에 B세포 표면 항원 단백질인 CD19를 인지할 수 있는 유전정보를 넣어준 후 다시 이 세포를 환자의 몸에 주입해 CD19를 발현하는 암세포를 인식해 사멸시키는 기전이다.
특히 면역관문수용체(T세포와 같은 면역세포의 기능을 억제해 면역 반응을 조절하는 역할을 하는 수용체)인 PD-1과 TIGIT의 발현을 억제함으로써 암세포의 면역 회피를 차단하고 T세포의 반응 강화 및 지속성을 유도해 항종양 효과를 높인 것이 특징이다.
림카토는 당초 3상 조건부허가를 신청했으나, 식약처는 허가 과정에서 3차 요법의 림프종 치료제로 사용되는 신규 CAR-T 제제임을 감안해 3상 임상시험을 면제했다. 대신 다른 글로벌 CAR-T 치료제와 마찬가지로 허가 후 장기추적조사와 위해성 관리계획 등을 통해 안전성과 유효성을 지속적으로 확인하는 조건으로 정식 허가했다.
식약처는 림카토주를 바이오챌린저(바이오의약품 마중물사업의 일환으로 혁신적인 개념과 기술을 가진 국내 개발 첨단바이오의약품에 대한 제품화 지원 프로그램) 대상 및 ‘글로벌 혁신제품 신속심사 지원체계(GIFT, 혁신성이 뛰어난 의약품을 시장에 출시해 환자에게 신속하게 공급하기 위한 식약처의 ‘글로벌 혁신제품에 대한 신속심사 활성화 지원체계)’ 제33호로 지정해 개발 초기 단계부터 단계별 맞춤형 상담과 신속심사를 통해 국내 혁신 항암제의 제품화를 지원했다.
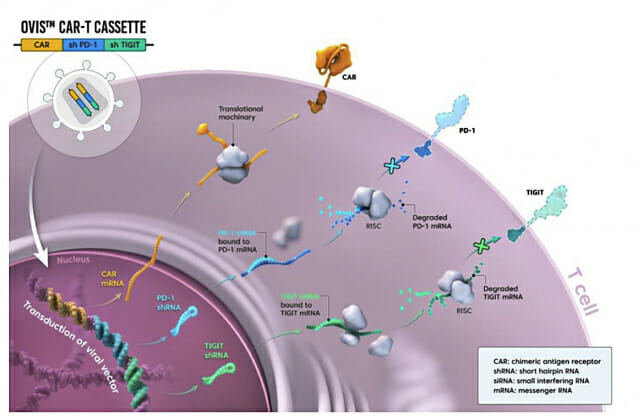
림카토는 큐로셀이 자체 개발한 OVIS(Overcome Immune Suppression) 기술이 적용된 CD19 CAR-T 치료제로, 종양 미세환경 내 면역억제 신호를 제어해 ‘T세포 탈진’(T-cell exhaustion) 문제를 개선하고, 항암 활성을 보다 장기간 유지하도록 설계됐다고 큐로셀 측은 설명했다.
이번 신약허가의 근거가 된 임상 2상 시험에서 림카토는 객관적 반응률(ORR) 75.3%, 완전관해율(CR) 67.1%를 기록했다. 또 안전성 측면에서도 CAR-T 치료의 대표 부작용인 중증 사이토카인 방출 증후군(CRS) 발생률 10%와 중증 신경독성(ICANS) 발생률 5%로 안전성을 확인했다.
관련기사
- 희귀 담도암 치료제 ‘지헤라주300mg’ 식약처 허가2026.03.19
- 큐로셀, 서울대로부터 고형암 치료용 ‘Hyperkine’ 기술 독점실시권 확보2025.11.10
- CAR-T 치료부터 남북 보건의료협력까지…혈액학의 현재와 미래 조망2025.11.06
- 큐로셀, 튀르키예 세포치료제 기업과 CAR-T 인프라 구축 협력2025.10.14
김건수 큐로셀 대표는 “림카토 허가는 우리나라 신약개발 역사에 커다란 이정표가 되었다. 지금까지 노력해 주신 많은 분들께 감사드린다”며 “CAR-T 기술의 불모지였던 국내에서 연구를 시작한 이후 첫 신약허가를 받게 됐다. 축적해 온 역량과 경험을 바탕으로 앞으로는 국내 CAR-T 기술의 글로벌 성공을 위해 최선을 다하겠다”고 말했다.
국내 개발 CAR-T 치료제에 대한 허가로 그간 고가의 해외 수입 제품에만 의존하던 CAR-T 치료제를 국내 기술로 직접 생산·공급할 수 있게 됨으로써 더 이상 치료 옵션이 없는 환자들에게 안정적인 치료 기회를 제공할 것으로 기대된다.