지난해 인‧허가된 의료기기 중 소프트웨어의 성장이 눈길을 끌었다.
식품의약품안전처가 발간한 ‘2022년 의료기기 허가보고서’를 분석한 결과, 인허가 상위 30개 품목 중 1등급 의료기기가 다수를 차지했고, 전체 의료기기 인허가 건수 감소추세에도 국내 제조품목 인허가 비중은 증가한 것으로 나타났다.
특히 의료기기 소프트웨어 건수 지속 증가했고, 국내 제조품목 강세를 보였으며, 임상시험자료 제출 대상 의료기기 허가 건수도 증가세를 유지했다. 반면 코로나19 특수에 급성장했던 체외진단의료기기는 전년 수준을 유지했다.
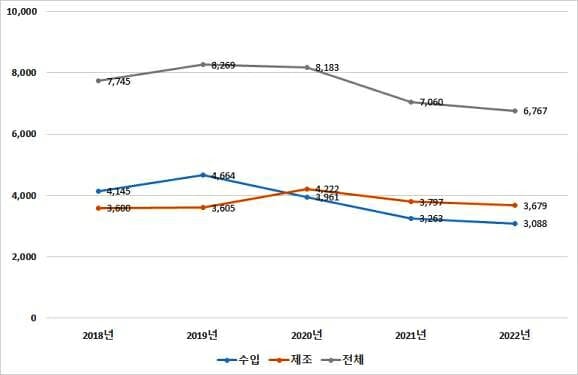
전체 의료기기 제조·수입품목 인허가는 코로나19 발생 이후 감소 추세이나 국내 제조품목의 비중은 지속적으로 증가하며 최근 3년간은 수입품목보다 높은 비율을 차지했다.
연도별 전체 인허가는 2018년 7천745건에서 2019년 8천269건, 2020년 8천183건, 2021년 7천60건, 2022년 6천767건(제조 853건, 수입 262건)으로 나타났다. 국내 제조 비중을 보면 2018년 46.5%, 2019년 43.6%, 2020년 51.6%, 2021년 53.8%, 2022년 54.4%로 증가 추세이다.
식약처는 국내 제조품목 인허가 비중 증가는 코로나19 유행이 지속되며 국내 우수한 기술력을 바탕으로 한 코로나19 진단시약 등 방역 관련 의료기기의 활발한 개발이 최근 3년 연속 국내 제조품목 증가에 영향을 미친 것으로 분석했다.
코로나19 관련 의료기기 제조 건수를 보면 2020년 448건에서 2021년 377건으로 감소했다가, 2022년 405건으로 다시 증가했다.
반면 수입품목의 인허가 건수는 2019년 4천664건에서 코로나19 발생 이후 2020년 3천961건, 2021년 3천263건, 2022년 3천88건(신고 2천240건, 인증 586건, 허가 262건) 등 매년 하락하고 있는데 이는 인허가 품목 중 신고·인증 품목의 감소가 주요 원인으로 보인다. 특히 수입 의존도가 높은 안경렌즈의 경우 수입인증건수가 2020년 825건(수입 302건)에서 2021년 600건(수입 75건), 2022년 586건(수입 69건)으로 가장 큰 감소 폭을 보였다.
의료기기 중 체외진단의료기기의 인허가 건수는 코로나19의 영향을 가장 크게 받은 것으로 나타났는데 2018년 945건(전체 의료기기의 12.2%)에서 2019년 760건(9.2%)으로 감소했다가 2020년 1천500건(18.3%), 2021년 1천36건(14.7%), 2022년 1천12건(15%)으로 일정 수준을 유지하고 있다.
체외진단의료기기는 다른 의료기기에 비해 허가가 높은 비율도 높았는데 지난해 코로나19 진단시약 149건 등 허가 370건, 인증 219건, 신고 423건으로 나타났다. 지난해 어린이 등의 사용 편의성이 높은 타액을 검체로 하는 자가검사키트 제품 3개가 처음으로 허가됐으며, 코로나19-독감(동시)진단시약 제품은 12개(PCR 2, 항원 10)가 허가됐다.
의료기기 소프트웨어의 경우 국내 제조품목이 강세를 보이며 지속적으로 증가하는 것으로 나타났다. 단독 소프트웨어 형태로 개발된 ‘의료기기 소프트웨어’는 2018년 20건에서 2019년 36건, 2020년 73건, 2021년 11건, 2022년 97건으로 나타났는데 2022년의 경우 국내 제조품목 83건으로 전체의 85.6%를 차지했다.
인공지능(AI) 기반 의료기기의 경우 소프트웨어가 강세를 보이고 있는데 2020년 44건(전체 50건), 2021년 37건(전체 37건), 2022년 41건(전체 48건) 등으로 높은 비중을 차지했다.
임상시험자료 제출 대상 의료기기의 허가 건수는 2020년 123건(1·2등급 37건, 3·4등급 86건), 2021년 133건(1·2등급 14건, 3·4등급 119건), 2022년 139건(1·2등급 15건, 3·4등급 124건)으로 증가세를 유지했다. 2022년의 경우 체외진단의료기기가 98건(79%)으로 가장 많았다.
식약처는 임상시험자료 제출 대상 의료기기가 최근 3년간 꾸준히 증가하고 있으며, 이는 고위험군인 3·4등급 의료기기에서 임상자료를 제출해야 하는 대상이 증가하고 있는 영향으로 보인다고 설명했다.
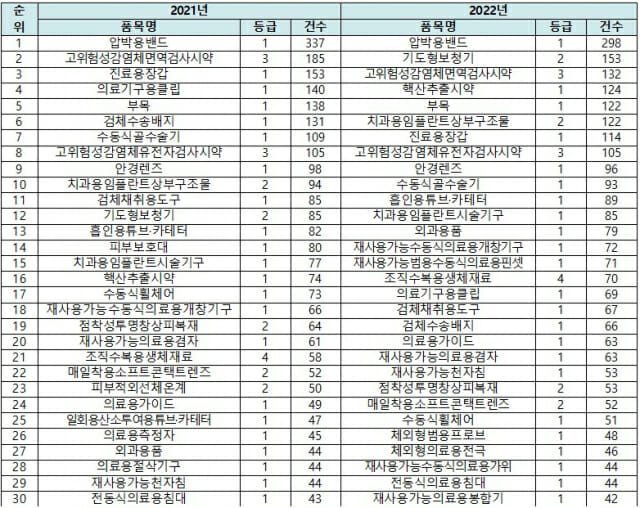
한편 2022년 인허가 건수 상위 30개 품목 중 1등급 품목은 ‘압박용밴드’ ‘핵산추출시약’ 등 23개 품목, 2등급 품목은 ‘기도형보청기’ ‘치과용임플란트상부구조물’ 등 4개 품목, 3등급 품목은 ‘고위험성감염체면역검사시약’ ‘고위험성감염체유전자검사시약’ 2개 품목, 4등급 품목은 ‘조직수복용생체재료’ 1개 품목 순으로 차지했다.









