차세대 항암 치료 방식으로 주목받는 면역항암제의 치료 성공률을 높이는 새로운 선천면역 조절 물질이 개발됐다. 이 물질은 암 세포 주변에 쉽게 침투할 수 있으며, 암 세포가 면역항암제에 더 잘 반응하게 만든다.
과학기술연구원(KIST, 원장 윤석진)은 KIST 뇌과학창의연구단 이상희 박사와 한국화학연구원 감염병치료제연구센터 김혜진 박사 연구팀이 선천면역 조절 단백질 'STING'에 대한 새로운 저분자화합물 기반 작용제를 개발했다고 18일 밝혔다.

STING은 DNA 병원체를 인지하여 인터페론을 분비하고 선천면역 반응을 조절하는 역할을 한다. 면역항암제의 일종인 면역관문억제제에 대한 암 세포의 반응성을 높이는데 활용할 수 있을 것으로 학계의 기대가 크다. 그러나 가장 먼저 임상이 진행된 STING 작용제 'ADU-S100'이라는 물질이 2020년 임상에서 중단되면서 새 작용제 개발이 시급한 실정이다.
연구진이 개발한 이 물질은 STING 단백질을 활성화, 면역반응에 관여하는 인터페론 등의 사이토카인 물질을 생성했다. 이어 이를 통해 T세포를 매개로 한 선천면역 반응을 유도했다.
선천면역 반응이 활성화되면서 종양의 면역표현형도 바뀌었다. 외부 위협 세포를 공격하는 T세포에 잘 반응하는 형태로 종양을 변화시킨 것이다. 정상 세포인 것처럼 위장한 암 세포가 면역세포에 잘 반응하지 않는다는 면역항암 치료의 문제를 개선했다.
그 결과, 동물모델 대상 실험에서 투여군의 20%는 암 세포가 완전히 사라졌다. 암 세포를 재이식해 암이 재발하는 환경을 유도한 경우에도, 추가적으로 약물을 투여하지 않아도 암 세포 성장이 억제되거나 아예 자라지 않았다.
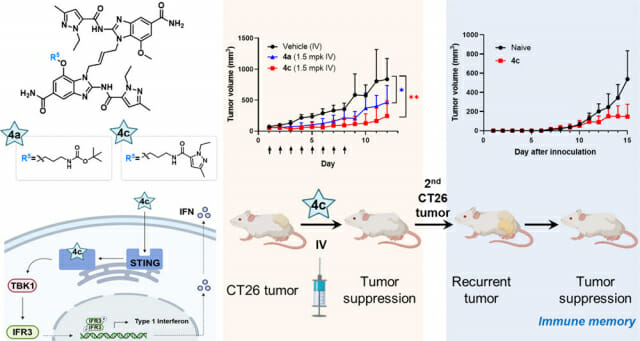
또 기존 STING 작용제는 종양에 직접 투여하는 방법이라 적용할 수 있는 암종이 제한적이지만, 이번에 개발된 물질은 정맥 투여가 가능해 이러한 한계를 극복했다.
관련기사
- '기적의 항암 치료' CAR-T에 날개 단다2022.04.09
- 펩타이드 접근성 조절 시스템 개발...환자맞춤형 면역 치료 실마리2022.03.13
- 단백질 모방한 나노머신이 암세포 뚫고들어가 죽인다2022.03.20
- "쿠팡 나와"...물 들어올 때 컬리로 노젓는 네이버2026.05.06
향후 방사선치료나 화학요법 등 기존 표준치료와 연계된 병용 치료요법, 나아가 항암을 위한 단독 투여로 활용될 수 있을 것으로 기대된다. 이상희 박사는 "이 연구가 뇌종양 등 임상에서 면역항암제 적용이 제한적인 암에 대한 새로운 치료전략 개발의 기반이 되기를 바란다"라고 밝혔다.
이 연구는 과학기술정보통신부 지원으로 KIST 주요사업, 한국화학연구원 주요사업과 한국연구재단 신진연구자지원사업 및 인공지능신약개발사업으로 수행됐다. 연구 결과는 의약화학 분야 학술지 '저널 오브 메디시널 케미스트리(Journal of Medicinal Chemistry)'에 게재됐다.












