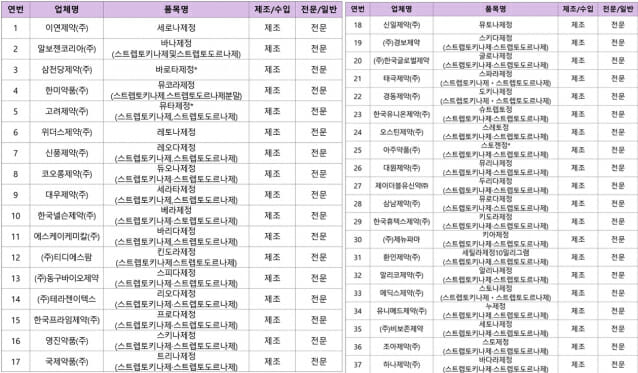
식품의약품안전처가 한미약품의 ‘뮤코라제정’ 등 ‘스트렙토키나제·스트렙토도르나제’ 제제 37개 의약품에 대해 사용중단 및 타 의약품으로의 대체를 권고했다.
식약처가 임상시험 재평가 결과에 따라 해당 품목들이 ‘호흡기 담객출 곤란’ 및 ‘발목 염증성 부종’에 대해 효과를 입증하지 못했다고 판단했다.
이에 따라 ‘의약품 정보 서한’을 이날 배포, 의·약사 등 전문가에게 ‘담객출 곤란’ 및 ‘발목 염증성 부종’ 환자에게 다른 의약품을 처방·조제하도록 협조 요청했다. 환자들에게도 이와 관련해 의·약사와 상의할 것을 당부했다.
보건복지부와 건강보험심사평가원 등에도 해당 품목의 의약품 정보 서한을 전달했다.
이는 허가받은 효능·효과를 입증하지 못한 ‘스트렙토키나제·스트렙토도르나제’ 제제에 대해 행정조치를 진행하기 이전에 일선 의료현장에서 사용되지 않도록 선제적으로 조치한 것이다.
한편, 식약처는 앞서 약사법 제33조에 따라 제제의 허가된 효능·효과에 대해 관련 업체에 국내 임상시험을 통해 최신의 과학 수준에서 효과성을 재평가하도록 명령했다. 이에 업체들은 동 제제에 대한 임상시험을 실시하고 그 결과를 제출했지만 효과를 입증하지는 못했다.
다만, 안전성에는 문제가 없는 것으로 알려졌다.












