식품의약품안전처는 통상 2∼3개월 걸리는 국가출하승인을 코로나19 백신에 대해서는 20일 이내로 단축할 계획이라고 29일 밝혔다.
식약처는 정부 코로나19 백신 접종 일정에 차질이 없도록 코로나19 백신을 신속출하승인 대상으로 지정해 다른 의약품보다 우선 처리할 예정이다.
식약처는 "코로나19 백신은 병원체나 항원단백질을 사용하던 기존의 백신과 달리 바이러스벡터, mRNA 등 유전물질을 사용하는 새로운 제조공정으로 만들어지므로 보다 철저한 국가출하승인이 필요하다"며 "식약처는 이를 위해 백신 허가 신청 전인 지난해 8월부터 제조사로부터 상세 시험방법과 시험법 밸리데이션 자료를 제출받아 국가출하승인 검정시험법을 마련하고 있다"고 설명했다.
이어 "통상적으로 2~3개월 이상 걸리는 국가출하승인을 20일 이내로 단축해 안전하게 접종할 수 있도록 백신을 공급할 계획"이라면서 "코로나19 백신 국내 공급을 위한 국가출하승인은 2월부터 시작될 예정"이라고 덧붙였다.
백신 신속출하 위해 작년 8월부터 준비
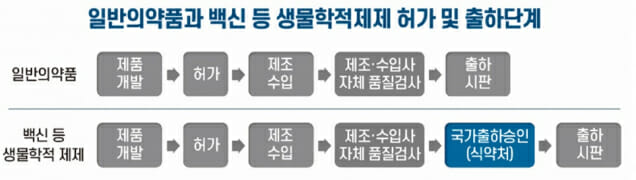
식약처는 백신의 경우 감염병 예방을 위해 영유아를 포함한 건강한 사람에게 단기간에 대규모로 접종하는 의약품으로, 제품 사용에 따른 파급력을 고려해 국가가 품질을 다시 한번 검증하는 국가출하승인 제도를 운영하고 있다. 백신 등 생물학적제제에 대한 제조단위 별 ‘검정시험’과 제조사가 허가받은 대로 제조하고 시험한 결과를 제출한 ‘자료검토’ 결과를 종합 평가하는 과정을 거친다.
검정시험은 백신의 품목별 특성을 고려해 안전성을 확인하기 위한 시험(무균시험, 엔도톡신시험 등)과 유효성을 확인하기 위한 시험(역가시험, 확인시험 등)을 실시하며, 필요한 경우 단백질함량시험, 함습도시험 등을 추가 실시한다.
예를 들어 아스트라제네카 백신의 경우 역가시험, 확인시험, 바이러스입자 함량시험 등 총 10종을, 화이자 백신의 경우 역가시험, 확인시험, 지질입자크기시험 등 12종을 검정시험 항목으로 예정하고 있다.
자료검토는 로트별 제조·시험기록이 의약품 제조·품질관리 기준(GMP)과 허가사항을 따르고 있는지 확인하는 것으로, 백신 원료(세포주, 바이러스주 등)부터 완제의약품까지의 제조·품질관리 시험기록의 적절성 등을 평가한다.
이에 식약처는 지난해 8월부터 백신 제조사로부터 상세 시험방법과 시험법 밸리데이션 자료 등을 제출받아 국가출사승인 검정시험법을 마련하는 등 신속출하승인을 준비 중이다.
관련기사
- 코로나19 백신 '일반 성인'은 언제 맞을 수 있나요?2021.01.28
- 코로나 백신 접종, 2월 의료진부터 7월 전국민 확대2021.01.28
- 9월까지 국민 70% 백신 접종…11월 집단면역 목표2021.01.26
- 2월 접종 유력 '화이자 백신' 해외서 어떤 효과?2021.01.25
특히 검정시험에 필요한 핵산추출기·나노입도분석기 등 첨단 분석장비를 긴급 구매하고 RNA백신 분석 실험실과 냉동보관 백신을 위한 보관품실 공사를 완료했으며, 국가출하승인 전문인력을 보강했다.
식약처는 아스트라제네카 백신에 대해 지난해 8월부터 검정시험에 필요한 상세 시험방법, 시약, 장비 등의 준비하여 지난해 12월 검정시험법을 마련했다. 화이자 백신에 대해서도 지난해 11월부터 시험방법, mRNA백신 분석 장비와 시약을 입수했다.









