"유럽의약품청(EMA), 미국 식품의약국(FDA)은 실제 환자에 대한 장기간의 약물 투여 결과 등 의료 현장에서 수집되는 데이터 기반 평가에 가치를 두기 시작했습니다. 이를 통해 과거 기준을 고수했다면 쓰이지 못했을 신약들도 허가승인을 받고 있습니다."
김정애 한국아이큐비아 상무는 19일 서울 강남구 삼정호텔에서 열린 '데이터3법 개정에 따른 보건의료 빅데이터 활용 방안 모색 토론회' 발제자로 나서 이같이 말했다.
지금까지는 약물의 장기 안전성 및 유효성을 평가하는 근거로 임상시험 데이터를 사용하는 게 일반적이었다.
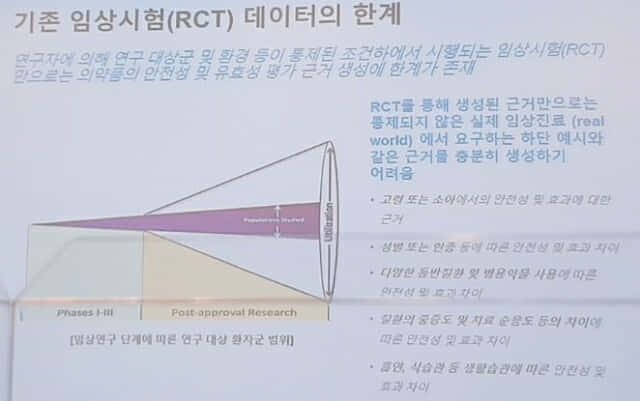
그러나 임상시험 데이터에는 한계가 존재한다. 우선 윤리적 이유로 임산부, 소아, 노인 등을 대상으로 한 임상시험이 불가하다. 희귀 질환도 모집단을 모으기가 어렵다. 또 5~10년에 걸쳐 대상자의 건강 상태를 추적하는 것도 현실적으로 거의 불가능하다.
EMA와 FDA는 이런 문제들을 해결할 수단으로 '실 사용 데이터'를 주목했다. 실 사용 데이터는 실제 의료환경에서 수집되는 데이터로 건강보험, 약국 자료, 웨어러블 기기에서 집계되는 데이터 등이 포함된다. 별도의 임상시험을 거치지 않고도 실 사용 데이터를 결합, 분석해 약물의 장기 안전성과 유효성을 검증하게 한 것이다.
이는 동시에 일정 규모 이상의 모집단을 모으기 어려운 희귀 질환 관련 데이터를 활용하기에 유리한 방법이다. 윤리적으로 임상시험이 허용되지 않는 집단에 대한 데이터를 수집하기에도 적합하다.
실제 의료 현장에서 다양한 환자들을 대상으로 얻은 데이터를 활용하는 만큼, 특정한 조건에서만 약효를 검증하는 임상시험 데이터 대비 환자별로 개인화된 데이터 분석을 제공할 수 있다는 장점도 있다. 이는 예방, 질병 예측에 집중하는 의료계 트렌드와도 맞아떨어진다는 설명이다.
김정애 상무는 실 사용 데이터를 활용해 EMA, FDA로부터 허가 승인을 받은 항암 치료제 '아벨루맙'을 언급했다. 아벨루맙은 희귀병인 전이성 메르켈 세포암 치료제 신약이다. 신약에 대한 직접비교 무작위 임상시험 데이터가 없었지만, 실제 환자 데이터와 아벨루맙 단일군 임상시험 결과를 비교한 데이터로 승인을 받아냈다.
임상시험이 어려운 소아 환자에 대한 활용 사례도 있다. 중추신경계 희귀질환 치료제인 특정 약물을 소아환자에게 투여해도 되는지 임상적으로 안전성과 유용성이 검증되지 못한 상태였지만, 유럽·아메리카·아프리카에서 얻은 실 사용 데이터로 투약을 승인받았다.
가임기 여성의 발병률이 높은 다발성 경화증도 핀란드와 스웨덴에서 수집된 실 사용 데이터로 임산부에 대한 투약이 허용됐다.
유럽에서는 이런 실 사용 데이터 활용을 뒷받침하는 인프라가 존재한다. 유럽 종양학 데이터 네트워크(ODN)이다. 유럽의 100개 이상의 병원 네트워크와 암 환자 8만여명에서 수집되는 데이터를 GDPR 기준에 맞춰 비식별화한 뒤 가입된 병원에게는 무료 분석, 활용을 허용한다. 비영리 단체, 사기업에게는 분석 결과를 받아볼 수 있게 했다.
관련기사
- 2.8조원 규모 바이오헬스 육성 사업 계획 예타 통과2020.07.03
- KISA, '첨단의료기기' 보안 강화 추진2020.05.26
- MS, 헬스케어 특화 클라우드 공개2020.05.21
- 美 직장인 코로나19 걸리면…"치료비 160만원"2020.03.18
김 상무는 우리나라에서 이런 보건의료 빅데이터 활용 사례가 다수 등장하기 위해서는 데이터의 표준화, 정형화, 구조화가 중요하다고 강조했다.
김 상무는 "실 사용 데이터는 연구용으로 만들어지지 않은 만큼 단독으론 가치가 떨어지는 등 장단점이 존재한다"며 "이런 한계를 보완하기 위해 서로 다른 데이터 간 연결이 반드시 필요하고, 이런 연결과 연결 과정에서의 데이터 보호를 위해 명확한 가이드라인이 나와야 한다"고 말했다.












