혈우병 유전자치료제가 국내 최초로 허가됐다.
식품의약품안전처(이하 식약처)는 씨에스엘베링코리아가 수입하는 희귀의약품 ‘헴제닉스주’(에트라나코진데자파르보벡)를 13일 허가했다고 밝혔다.
B형 혈우병은 혈액 응고에 관여하는 인자 중 혈액응고 제9인자의 일부 또는 전체 결핍으로 출혈 가능성이 증가하는 선천성 유전질환이다.
헴제닉스주는 혈액응고 제9인자를 암호화하는 DNA 서열을 간세포에 도입해 간세포에서 혈액응고 제9인자를 생산하도록 하는 작용하며, 혈액응고 제9인자에 대한 억제인자(FIX Inhibitor)가 없는 성인의 중증에 가까운 중등증 및 중증 B형 혈우병(선천성 혈액응고 제9인자 결핍) 치료에 허가됐다.
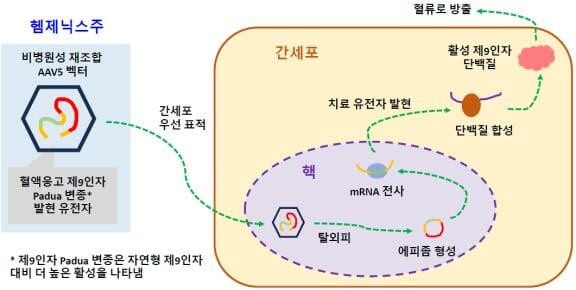
기존 치료제와 달리 장기적인 치료를 목적으로 단회 투여하여 B형 혈우병 환자에게 새로운 치료 기회를 제공할 것으로 기대된다.
관련기사
- JW중외제약, 혈우병 치료제 ‘헴리브라’ 투약자 50% 무출혈 신체활동2024.01.18
- AI, 추론 모델→행동도구로…'월드모델' 경쟁 불붙는다2025.12.22
- 침체된 韓 극장가, 물 건너온 애니메이션이 살렸다2025.12.22
- 로봇이 차 만들고 로봇개가 품질검사…현대차그룹 '제조혁신' 가속2025.12.22
식약처는 ‘헴제닉스주’의 품질, 안전성·효과성, 제조 및 품질관리기준 등을 첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률(이하 첨단재생바이오법)에서 정한 심사기준에 따라 과학적으로 철저하게 심사·평가하면서, 신속처리 대상으로 지정해 의료현장에 빠르게 도입될 수 있도록 노력했다고 밝혔다.
또 헴제닉스주는 첨단재생바이오법 제30조에 따른 ‘장기추적조사’ 대상 의약품으로 제약사가 투여일로부터 15년간 이상사례 발생 현황을 추적조사하는 등 첨단바이오의약품 안전관리에 만전을 기하겠다고 덧붙였다.












